ARTÍCULOS

Uso de la piel de cerdo liofilizada en el lesionado quemado
Use of freeze-dried pig skin in burn injuries
Autor: Dra. Carolina Lara Cedillo (ORCID 0009-0001-5453-947X)
Sobre el autor: Médica, residente de segundo año de la especialidad de Cirugía Plástica y Caumatología
Información del manuscrito: Recibido/Received: 29-01-25
Aceptado/Accepted: 06-05-25
Contacto de correspondencia: laracedillo0@gmail.com
Resumen
Introducción: Las quemaduras son un problema de salud pública mundial y causa importante de morbilidad y mortalidad. El propósito del tratamiento de las quemaduras es asegurar la rápida epitelización tanto superficial como profunda. El objetivo de la presente revisión es presentar de manera estructurada la información sobre el tratamiento del paciente quemado con especial atención en los apósitos, en particular los de piel de cerdo. Metodología: Se realizó la búsqueda en bases de datos como PubMed, Scielo y Google académico, sin restricción de idioma. En dicha búsqueda se emplearon los términos: quemado, piel de cerdo liofilizada y tratamiento de quemados. La selección de los artículos se realizó en base a los títulos y los resúmenes. La sistematización incluyó artículos originales y de revisión, ensayos controlados aleatorizados, informes de casos y ensayos clínicos. Resultados: Los apósitos deben lograr apoyar principalmente el proceso de regeneración tisular, proteger contra infecciones y reducir la incomodidad del paciente durante los cambios de apósito, lo que incluye minimizar el dolor y los costos del tratamiento. Entre los apósitos empleados con este fin se encuentran los derivados de la piel de cerdo, los cuales presentan propiedades muy semejantes a los apósitos de piel humana, en cuanto a la disposición del colágeno, la histología, reacción inmunológica y su biocompatibilidad, así como que su utilización temporal en el manejo auxiliar de la cicatrización en quemaduras es satisfactoria, en términos de tiempo de cicatrización, con un rendimiento al menos no inferior al mejor de los tratamientos estándar. Conclusiones: Los apósitos de piel de cerdo liofilizada muestran resultados satisfactorios en la aplicación temporal sobre quemaduras en humanos y resultan útiles en el apoyo de la cicatrización, dados por las similitudes estructurales y el nivel de biocompatibilidad que estos apósitos muestran con relación al ser humano.
Palabras clave: lesionado quemado, piel porcina, apósitos.
Abstract
Introduction: Burns are a global public health problem and a major cause of morbidity and mortality. The purpose of burn treatment is to ensure rapid superficial and deep epithelialization. The objective of this review is to present information on the treatment of burn patients in a structured manner, with special attention to dressings, particularly those made from pig skin. Methodology: A search was conducted in databases such as PubMed, Scielo, and Google Scholar, without language restrictions. The search terms used were burn, freeze-dried pig skin, and burn treatment. Articles were selected based on their titles and abstracts. The systematization included original and review articles, randomized controlled trials, case reports, and clinical trials. Results: Dressings should primarily support the tissue regeneration process, protect against infection, and reduce patient discomfort during dressing changes, including minimizing pain and treatment costs. Among the dressings used for this purpose are those derived from pig skin, which have properties very similar to human skin dressings in terms of collagen arrangement, histology, immune response, and biocompatibility. Their temporary use in the auxiliary management of burn healing is satisfactory in terms of healing time, with performance at least equal to the best standard treatments. Conclusions: Freeze-dried pig skin dressings show satisfactory results in temporary application to human burns and are useful in supporting healing, given the structural similarities and level of biocompatibility that these dressings show in relation to humans.
Keywords: Injured burns, porcine skin, dressings
Introducción
La piel es el órgano más grande del cuerpo y garantiza la homeostasis del organismo. La pérdida de su integridad puede provocar alteraciones de las funciones termorreguladora y protectora frente a factores externos nocivos como microorganismos, radiaciones o cambios de temperatura y aumentar el riesgo de infecciones, pérdida de agua, hipotermia e incluso la muerte del organismo (1).
Las quemaduras constituyen eventos complejos desde el punto de vista fisiopatológico y terapéutico. Se trata de un trauma, que causa alteraciones hístico-humorales en correspondencia con la magnitud del trauma; cuando esta es extensa, puede sobrepasar los efectos locales y repercutir sobre los órganos y sistemas (2,3), ya que se producen alteraciones en los mecanismos sistémicos de defensa del huésped (4,5,6).
Las quemaduras pueden afectar a las distintas capas de la piel, y a lo largo de los años se han propuesto diferentes clasificaciones según la profundidad de las mismas. La clasificación más actual que se emplea en el gremio es la siguiente:
- Epidérmicas o de primer grado
- Dérmicas A o de segundo grado superficial
- Dérmicas B o de segundo grado profundo
- Hipodérmicas o de tercer grado (7)
En Europa, las quemaduras se dividen con mayor frecuencia en superficiales, dérmicas profundas y de espesor total. Las quemaduras superficiales suelen ser rojas, secas y dolorosas. Afectan solo a la epidermis y se curan espontáneamente mediante su regeneración en aproximadamente siete días (8).
Las quemaduras superficiales de espesor parcial afectan a la parte superficial de la dermis. Suelen ser rojas, húmedas, con ampollas y suelen ser muy dolorosas. Con el tratamiento adecuado, también pueden curarse por sí solas en 14 días (8).
Las quemaduras dérmicas profundas se extienden a la dermis, dañando los folículos pilosos y el tejido glandular, tienen la capacidad de curarse espontáneamente en un plazo de dos a tres semanas, especialmente después del desbridamiento enzimático; sin embargo, a menudo es necesario cerrar la herida de forma temprana con injerto de piel para evitar la formación de cicatrices hipertróficas y contracturas. Las quemaduras de espesor total con tejido subcutáneo subyacente no cicatrizan espontáneamente y también requieren tratamiento quirúrgico (8).
La Organización Mundial de la Salud, en su reporte de 2018, planteó que las quemaduras constituyen un problema de salud pública a nivel mundial y provocan alrededor de 180,000 muertes al año, la mayoría se producen en los países de bajos y medianos recursos y casi dos tercios en África y Asia Sudoriental, mientras que en muchos países de altos ingresos la tasa de muertes por quemaduras ha disminuido en los últimos años (8).
Actualmente las quemaduras ocupan el cuarto lugar dentro de las lesiones traumáticas en el mundo, con una amplia variabilidad en la incidencia y en la supervivencia de las lesiones extensas, lo cual depende del desarrollo del país (9-12).
La atención de los lesionados quemados es un gran desafío para el personal médico, debido a diversos factores como: situación clínica, evolución, presencia de enfermedades asociadas, la gran variedad de tratamientos existentes, infraestructura e insumos médicos, tiempo de permanencia en hospitalización, el elevado costo económico y social que implican, entre otros factores (13).
El proceso de cicatrización de las heridas implica hemostasia, inflamación, proliferación y remodelación. A diferencia de las quemaduras superficiales, que se curan de forma automática y rápida sin dejar cicatrices predecibles, las quemaduras profundas suelen afectar a las funciones de las células cutáneas después de la infección, lo que provoca una inflamación excesiva y una deposición anormal de colágeno debido al microambiente hipohidratado. Estas complicaciones pueden provocar un retraso en la cicatrización, falta de cicatrización, cicatrices y desfiguración (14).
Dependiendo de la fase de la quemadura, el estado del paciente y la causa de la misma, se debe elegir el tratamiento adecuado de manera individualizada. Con el uso de la piel de cerdo liofilizada, se intenta llevar al paciente lo más temprano posible a sala de operaciones y bajo anestesia general, lograr, primero, una limpieza exhaustiva y un diagnóstico más exacto de la extensión y profundidad según superficie corporal quemada (SCQ), y segundo, realizar las escarectomías tangenciales necesarias hasta encontrar tejido húmedo y cubrir toda lesión con piel de cerdo liofilizada rehidratada (15).
La mayor parte de los avances se han producido en el campo de los biomateriales y la ingeniería de tejidos, pero todavía no se ha desarrollado un biomaterial ideal que imite la estructura de la piel y sea capaz de restaurar la función cutánea, la pigmentación, los apéndices cutáneos, los vasos y los nervios y se necesitan ensayos aleatorios en grandes poblaciones para evaluar la eficacia de las terapias experimentales utilizando nuevos apósitos y sustitutos de la piel (16).
Se considera que no existe un apósito para quemaduras que proporcione una curación completa sin múltiples cambios del mismo, cirugía adicional e injertos de piel. El tratamiento implica varias etapas, incluidas medidas conservadoras para el shock de la quemadura y la protección de la herida, seguidas de procedimientos quirúrgicos como la escisión de tejido y el cierre con injertos de piel (17) o mediante enfoques conservadores con apósitos especializados como hidrogeles, hidrocoloides o técnicas de limpieza enzimática (18). Con la aplicación de estos apósitos se evita la fuga exagerada de agua y revaporización a través de las zonas quemadas; disminuye la alteración electrolítica y el dolor, permitiendo la movilización activa y pasiva de las articulaciones; limita el crecimiento bacteriano, favoreciendo definitivamente, el desarrollo de la granulación de los tejidos (19).
Objetivos
- Profundizar en las bondades de los apósitos de piel de cerdo en el tratamiento del lesionado quemado.
- Sistematizar los resultados de la utilización de piel de cerdo liofilizada en el tratamiento de lesionados quemados.
Metodología
En la presente revisión sistemática se recopilan estudios que tienen como objetivo describir de manera lógica los resultados en la utilización de la piel de cerdo liofilizada en el tratamiento de lesionados quemados.
Los criterios de selección se basaron en artículos originales y de revisión, ensayos controlados aleatorizados, informes de casos y ensayos clínicos, en base a los títulos y los resúmenes de fuentes documentales como PubMed, Google Académico y Scielo, sin restricción de idioma, utilizando como palabras claves, lesionado quemado, piel porcina y apósitos.
Se incluyeron los artículos con acceso al texto completo, que permitieron evaluar la correspondencia entre resumen y escrito. Se excluyeron las repeticiones. Los criterios de selección para la inclusión/exclusión fue evaluada de manera individualizada, teniendo en cuenta los aspectos de novedad, pertinencia y relevancia. Se filtraron 256 artículos y se seleccionó para la revisión el 30 % de ellos, que se ordenaron cualitativamente por tema, a partir de un análisis de variabilidad, fiabilidad, actualidad y validez de la información.
Resultados
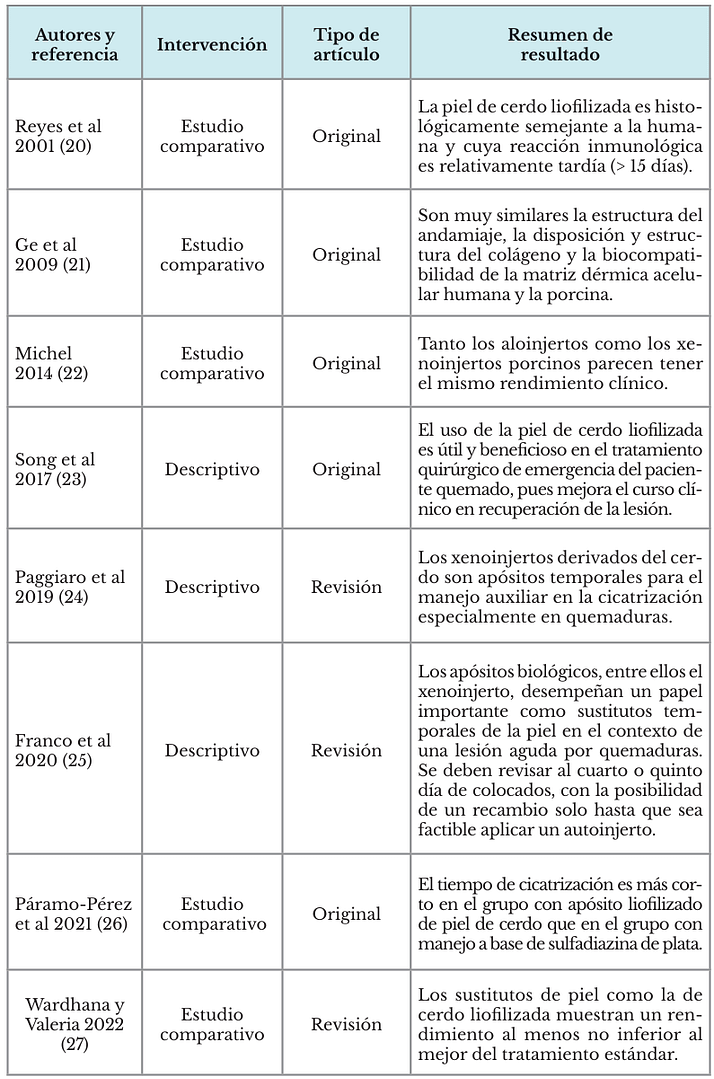
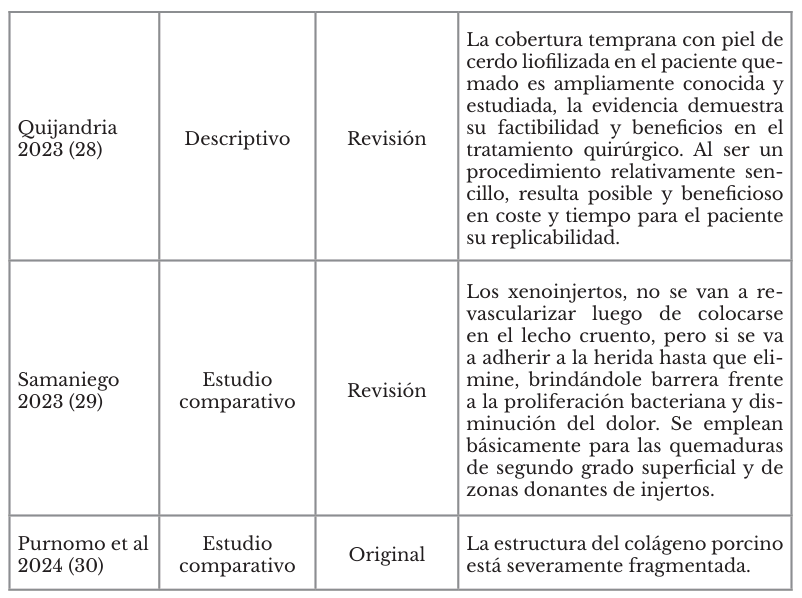
Después de una búsqueda extensa de artículos, finalmente se incluyeron once, en los cuales se pudo determinar que la piel de cerdo liofilizada es histológicamente semejante a la humana. Su reacción inmunológica es relativamente tardía al aplicarse en humanos, son similares en la estructura del andamiaje, la disposición y estructura del colágeno y la biocompatibilidad de la matriz dérmica celular humana y la porcina, lo que apoya los resultados clínicos de la aplicación de estos apósitos en humanos con lesiones por quemaduras. Tanto los aloinjertos como los xenoinjertos porcinos parecen tener el mismo rendimiento clínico; el tiempo de cicatrización es menor con apósito liofilizado de piel de cerdo que con la sulfadiazina de plata y que los sustitutos de piel de cerdo liofilizada muestran un rendimiento al menos no inferior al tratamiento estándar, así los xenoinjertos derivados del cerdo son apósitos temporales útiles para el tratamiento auxiliar en la cicatrización, especialmente en lesiones por quemaduras (Tabla 1).
Tabla 1. Estudios relevantes incluidos en la revisión
Fuente: (Villatoro, 2025).
Desarrollo y Discusión
En la sistematización realizada se pudo identificar que las quemaduras son un problema de cuidados críticos frecuentes y las prioridades de su tratamiento se centran en estabilizar al paciente, prevenir infecciones y optimizar la recuperación funcional, por lo que garantizar una rápida epitelización en las quemaduras superficiales y el proceso de reconstrucción de la piel perdida en las quemaduras profundas, involucra, en muchos casos, la utilización de sustitos dérmicos, aspecto referido en la presente revisión.
Diferentes estudios plantean que la utilización de la piel de cerdo liofilizada es una buena opción para el tratamiento de las quemaduras. Autores como Reyes et al 2001 (20), Ge et al 2009 (21), Michel 2014 (22) y más reciente, Paggiaro et al 2019 (24) plantean que por sus características histológicas son semejantes a la piel humana, y los resultados de su aplicación desde el punto de vista clínico son semejantes a los del homoinjerto, y su utilización como apósitos temporales puede ser considerado de gran utilidad, criterio con el que coincide esta autora, teniendo en cuenta que la piel de cerdo liofilizada empleada como sustituto temporal de la piel actúa como apósito biológico que separa el medio externo del interno y esto ayuda a prevenir infecciones y favorece el proceso de cicatrización.
Este aspecto es corroborado por el criterio de Rowan et al (31), cuando plantea que los injertos de piel autólogos de espesor parcial son el método principal para cerrar quemaduras de piel de espesor completo, pero la falta de sitios donantes puede prolongar el proceso de curación y reducir este tiempo, lo que traería consigo beneficios por lo que, para este propósito, se desarrollan materiales biológicos y sintéticos.
Por otra parte, se hace referencia a que el tratamiento tópico juega un papel importante en este proceso, ya que tiene como objetivo crear condiciones óptimas para la regeneración espontánea del defecto cutáneo o la preparación de las heridas para el trasplante después de la eliminación de los tejidos necróticos. La creación de condiciones óptimas para la curación implica, entre otros aspectos, la eliminación de fibrina, tejidos necróticos y secreciones excesivas de la superficie de la herida, y la aplicación de los apósitos temporales protege los tejidos de la desecación asegurando una humedad constante (32,33).
A criterio de esta autora, mientras mejor preparada esté la piel al momento del injerto, más favorable será el resultado en la cicatrización y recuperación final del lesionado quemado, todo ello se revierte en una mejor calidad de vida del paciente, disminución del sufrimiento tanto físico como psicológico y mejores resultados funcionales y estéticos.
Shahrokhi (34), describe que los sustitutos de piel son cubiertas cutáneas temporales o permanentes que se utilizan en el tratamiento de heridas agudas y crónicas. Los sustitutos de la piel pueden ser de origen biológico, sintético o biosintético, y suelen estar indicados para heridas crónicas, como úlceras diabéticas o venosas, o heridas agudas, como las lesiones por quemaduras. El uso de sustitutos de la piel puede mejorar las tasas de cicatrización de heridas, así como los resultados cosméticos y funcionales.
Franco (25) realiza un estudio descriptivo, tipo serie de casos, donde se incluyeron 60 pacientes con quemaduras cuyo tratamiento fue cirugía con piel de cerdo liofilizada, el 75 % de las quemaduras fueron causadas por líquidos calientes. La media de la Superficie Corporal Quemada (SCQ) fue de 8.8 %; el 96.7 % de lesiones no se infectaron y la duración en días promedio de hospitalización fue de ocho, realizando 2.5 operaciones por paciente. Con recuperación total estética de 41.7 % y funcional de 91.7 %. Con sensación de bienestar luego del tratamiento 98 %. Concluyendo que este tipo de tratamiento fue de beneficio para los pacientes del estudio, criterio con el que coincide esta autora, dada las bondades de la piel de cerdo liofilizada.
Otros autores como Shoham et al (35), y Korzeniowski et al (36), coinciden en que no se han desarrollado apósitos ideales para el tratamiento de las heridas por quemaduras profundas, que permitan su curación completa sin la necesidad de múltiples cambios de apósito, intervenciones quirúrgicas adicionales y el cierre definitivo de los defectos cutáneos con injertos de piel de espesor parcial.
El tema tratado en la presente revisión debe ser considerado como vigente en la investigación científica por la publicación de diferentes autores en años recientes. A criterio de esta autora, se ha demostrado la factibilidad y beneficios en el tratamiento quirúrgico de lesionados quemados, con la utilización de piel de cerdo liofilizada.
Bay et al (37), en el 2021 refieren que, en la actualidad existen 76 productos sustitutos de la piel disponibles en el mercado, este artículo proporciona una revisión de la literatura relevante relacionada con las principales categorías de sustitutos de la piel disponibles.
Korzeniowski et al (36) en el 2022 y Barbachowska et al (32) en el 2023, reseñan que un apósito seleccionado para el tratamiento de quemaduras dérmicas profundas debe apoyar el proceso de regeneración tisular, proteger contra infecciones y reducir la incomodidad del paciente, lo que incluye minimizar el dolor y los costos del tratamiento.
Estos materiales son una opción terapéutica en quemaduras superficiales y de espesor parcial superficial. Se necesitan más ensayos clínicos aleatorizados, realizados en varios centros para reafirmar y corroborar los efectos a mediano y largo plazo, así como la influencia precisa en el desarrollo de la cicatriz.
Si bien, en la literatura médica revisada hay consenso en la utilización de piel de cerdo y el aseo quirúrgico inmediato con la realización del autoinjerto lo más precoz posible, de igual manera, persiste la incertidumbre de cuando realizar la escarectomía tangencial sobre todo en pacientes con áreas extensas de quemaduras, teniendo como factores limitantes el sangrado y la descompensación que produce este procedimiento, y la falta de área dadora para la cobertura total SCQ.
Un estudio realizado en México plantea que el tiempo de cicatrización fue más corto en el grupo tratado con apósito liofilizado de piel de cerdo (10.2 semanas) que en el grupo tratado a base de sulfadiazina de plata (13.8 semanas). Páramo (26) plantea que a las 9 semanas de iniciado el tratamiento, la mitad de los pacientes con apósito de piel de cerdo ya habían cicatrizado, comparado con la cicatrización en el grupo tratado con sulfadiazina de plata (20 %). La probabilidad de cicatrización a las 11 semanas en paciente manejados con sulfadiazina de plata es 20 % y con apósito liofilizado de piel de cerdo 80 %. El apósito liofilizado de piel de cerdo tuvo mejores resultados, comparados con el manejo estándar con sulfadiazina de plata (26). A criterio de esta autora, se hace necesario realizar estudios aleatorizados para demostrar la efectividad de este material como herramienta terapéutica.
Conclusión
Los apósitos de piel de cerdo liofilizada muestran resultados satisfactorios en la aplicación temporal sobre quemaduras en humanos y resultan útiles en el apoyo de la cicatrización, dados por las similitudes estructurales y el nivel de biocompatibilidad que estos apósitos muestran con relación al ser humano.
Son necesarios también estudios multicéntricos que evalúen los diferentes sustitutos que existen; las publicaciones son tan disímiles que no permiten una adecuada comparación para obtener conclusiones con verdadera evidencia.
Bibliografía
- Atiyeh BS, Gunn SW, Hayek SN. State of the Art in Burn Treatment. Mol. Med. 2005, [Consultado el 22 de diciembre de 2022], 29, p. 131–148. Disponible en: https://www.ncbi.nlm.nih.gov/pubmed/15654666
- Borges MH, García RR. Manual de procedimientos de diagnóstico y tratamiento en Caumatología y Cirugía Plástica. La Habana: Editorial Pueblo y Educación; 1984. p. 31-3. Disponible en: https://catalogo.hlg.sld.cu/index.php?P=FullRecord&ID=9084&ReturnText=Search+Results&ReturnTo=index.php%3FP%3DAdvancedSearch%26Q%3DY%26G80%3D195
- Rivera EF. Abordaje global y tratamiento local de quemaduras en adultos: revisión bibliográfica. [Tesis de titulación]. 2022. Disponible en: https://dspace.ucacue.edu.ec/bitstream/ucacue/12568/1/9BT2022-MTI071-Rivera%20Suco%2C%20Edwin%20Fabricio.pdf
- Nielson CB, Duethman NC, Howard JM, Moncure M, Wood JG. Burns: pathophysiology of systemic complications and current management. J. BurnCare Res. 2017; 38: e469–e481. Disponible en: https://academic.oup.com/jbcr/article-abstract/38/1/e469/4568966
- Moran AT, Cerro SJ, Tapia ZC, Castillo OL, Apolo YG, Lema RA, et al. Abordaje terapéutico del paciente quemado: importancia de la resucitación con fluido terapia. Archiv Venez Farmac Terapeut 2019; 38(1): [aprox. 10 p]. Disponible en: http://saber.ucv.ve/ojs/index.php/rev_aavft/article/view/16410
- Radzikowska-Büchner E, Łopuszyńska I, Flieger W, Tobiasz M, Maciejewski R, Flieger J. An Overview of Recent Developments in the Management of Burn Injuries. Int J Mol Sci. 2023 Nov 15; 24(22): 16357. doi: 10.3390/ijms242216357
- Soler Vaillant R, Mederos Curbelo ON. Cirugía. Tomo II. Afecciones quirúrgicas frecuentes [Internet]. La Habana: Editorial Ciencias Médicas; 2018. Disponible en: http://www.bvscuba.sld.cu/libro/cirugia-tomo-ii-afecciones-quirurgicas-frecuentes/
- Quemaduras. Datos y cifras. Organización Mundial de la Salud. 2018. Disponible en: https://www.who.int/es/news-room/fact-sheets/detail/burns
- Davies K, Johnson EL, Hollén L, Jones HM, Lyttle MD, Maguire S, et al. Incidence of medically attended paediatric burns across the UK. Inj. Prev. 2020; 26: p. 24–30. Disponible en: https://injuryprevention.bmj.com/content/26/1/24.abstract
- Asena M, Aydin P, Ozturk U. Sociodemographic and culture results of paediatric burns. Int. Wound J. 2020; 17: p. 132–136. Disponible en: https://onlinelibrary.wiley.com/doi/abs/10.1111/iwj.13244
- Miricescu D, Badoiu SC, Stanescu-Spinu II, Totan AR, Stefani C, Greabu M. Growth factors, reactive oxygen species, and metformin-promoters of the wound healing process in burns? Int. J. Mol. Sci. 2021; 22: 9512. Disponible en: https://doi.org/10.3390/ijms22179512
- Jeschke MG, Van Baar ME, Choudhry MA, Chung KK, Gibran NS, Logsetty S. Burn injury. Nat Rev Dis Primers. 2020; 6(1): p. 11. Disponible en: doi: 10.1038/s41572-020-0145-5. PMID: 32054846; PMCID: PMC7224101
- Castillo P. Quemaduras. Conceptos para el médico general. Cuadernos de cirugía, 2003; 17(1), p. 58-63. Disponible en: http://revistas.uach.cl/index.php/cuadcir/article/view/2256
- Chen S, Xiong Y, Yang F, Hu Y, Feng J, Zhou F, et al. Approaches to scarless burn wound healing: application of 3D printed skin substitutes with dual properties of anti-infection and balancing wound hydration levels. EBioMedicine. 2024; 106: 105258. Disponible en: doi: 10.1016/j.ebiom.2024.105258
- Muñoz B, Suárez-Sánchez R, Hernández-Hernández O, Franco-Cendejas R, Cortés H, Magaña JJ. From traditional biochemical signals to molecular markers for detection of sepsis after burn injuries. Burns 2019; 45(1): p. 16-31. Disponible en: https://doi.org/10.1016/j.burns.2018.04.016
- National Burn Repository. Update, Report of Data from 2009–2018. American Burn Association NBR Advisory Committee. Dataset Version 14.0. Ameriburn.siteym.com.2019; 2019. Disponible en: https://www.who.int/publications/i/item/9789240011311
- Gacto-Sanchez P. Surgical treatment and management of the severely burn patient: Review and update. Med. Intensiva 2017; 41: p. 356–364. Disponible en: https://www.sciencedirect.com/science/article/pii/S2173572717301170
- Markiewicz-Gospodarek A, Kozioł M, Tobiasz M, Baj J, Radzikowska-Büchner E, Przekora A. Burn Wound Healing: Clinical Complications, Medical Care, Treatment, and Dressing Types: The Current State of Knowledge for Clinical Practice. Int. J. Environ. Res. Public Health 2022; 19: 1338. Disponible en: https://www.mdpi.com/1660-4601/19/3/1338
- Mansoor El, Harrazin M. Burns in children: Early versus late excision and grafting. Professional Med J 2012 [Consultado 18 de diciembre de 2024]; 19(5): p. 625-629. Disponible en: https://www.tandfonline.com/doi/abs/10.1185/03007997809110213
- Reyes ML, Gonzales C, Flores M, Peralta J, Reyes J, Reboyo D, Rodríguez MD. Apósitos de Piel de Cerdo deshidratados por liofilización. Banco de Tejidos Radio esterilizados, Instituto Nacional de Investigaciones Nucleares 2001 [Consultado: 13 de abril de 2025]. Disponible en: https://inis.iaea.org/collection/NCLCollectionStore/Public/39/015/39015113.p
- Ge L, Zheng S, Wei H. Comparison of histological structure and biocompatibility between human acellular dermal matrix (ADM) and porcine ADM. Burns. 2009 [Consultado: 13 de abril de 2025]. 35(1): p. 46-50. Disponible en: https://www.sciencedirect.com/science/article/pii/S0305417908001447
- Michel H.E. Hermans, Porcine xenografts vs. (cryopreserved) allografts in the management of partial thickness burns: Is there a clinical difference? Burns, 2014 [Consultado: 13 de abril de 2025]; 40(3): p. 408-415. Disponible en: https://doi.org/10.1016/j.burns.2013.08.020
- Song DH, Neligan PC. Plastic Surgery, 4th ed.; Trunk and Lower Extremity; Elsevier: Amsterdam, The Netherlands, 2017. Disponible en: https://books.google.es/books?hl=es&lr=&id=cR0xDwAAQBAJ&oi=fnd&pg=PP1&dq=Song,+D.H.%3B+Neligan,+P.C.+Plastic+Surgery&ots=NMTwuEjRSa&sig=qYR1QiSulynuEbyCGj4IZNYHoSw
- Paggiaro AO, Bastianelli R, CarvalhoVF, Isaac C, Gemperli R. Allograft skin, the gold-standard for burn skin substitute? A systematic literature review and metaanalysis. Journal of Plastic, Reconstructive & Aesthetic Surgery 2019; 72: p. 1245-53. Disponible en: doi:10.1016/j.bjps.2019.04.013
- Franco ER, Saravia JH, Alfaro PR. Piel de cerdo liofilizada en tratamiento de quemaduras: Serie de casos 2014-2016. Rev. Tzhoecoen. Julio-septiembre 2020. Vol. 12 / Nº 3, p. 315-324.ISSN: 1997-873. Disponible en: https://revistas.uss.edu.pe/index.php/tzh/article/view/1329/1267
- Páramo-Pérez M, Pérez-González HA, Villareal-Ríos E Flores-Lara D, Herrera-González M, Solis-López A. Utilidad del apósito liofilizado de piel de cerdo en el manejo de cicatrización de úlcera de pie diabético. Rev. cir. 2021; 73(6): p. 691-698. Disponible en: http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S245245492021000600691&lng=es.
- Wardhana A, Valeria M. Efficacy of skin substitutes for management of acute burn cases: a systematic review. Ann Burns Fire Disasters. 2022; 30; 35(3): p. 227-236. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10067142/pdf/Ann-Burns-and-Fire-Disasters-35-227.pdf PMID: 37016595; PMCID: PMC10067142
- Quijandria AP. Factibilidad del injerto con piel de cerdo liofilizada en el tratamiento quirúrgico de quemaduras en el contexto de un Servicio de Salud Peruano. Acta Médica Peruana. 2023. DOI:10.35663/amp.2023.403.2471
- Samaniego LA. Beneficios clínicos de xenoinjerto piel porcina. Tesis. 2023. Universidad de San Martín de Porres. Disponible en: https://hdl.handle.net/20.500.12727/12391
- Purnomo AT, Syarif AN, Wardhana A, Siregar NC. Comparative study of striped catfish (Pangasiushypophthalmus) skin, Nile tilapia (Oreochromisniloticus) skin, and porcine skin as a xenograft material for burn wound. Ann Burns Fire Disasters. 2024 30; 37(3): p. 242 249. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC11372273/
- Rowan MP, Cancio LC, Elster EA, Burmeister DM, Rose LF, Natesan S, et al. Burn wound healing and treatment: Review and advancements. Crit. Care 2015; 19: p. 243. Disponible en: https://doi.org/10.1186/s13054-015-0961-2
- Barbachowska A, Korzeniowski T, Surowiecka A, Strużyna J. Alloplastic Epidermal Skin Substitute in the Treatment of Burns. Life (Basel). 2023; 14(1): p. 43. Disponible en: doi:10.3390/life14010043. PMID: 38255658; PMCID: PMC10821452.
- Shoham Y, Krieger Y, Rubin G, Koenigs I, Hartmann B, Sander F, et al. Rapid enzymatic burn debridement: A review of the paediatric clinical trial experience. Int. Wound J. 2020; 17: p. 1337-1345. Disponible en: https://doi.org/10.1111/iwj.13405
- Shahrokhi S. Skin substitutes. In: Jeschke MG, Collins KA, eds. UpToDate. UpToDate; february 22, 2021. Disponible en: https://www.uptodate.com/contents/skin-substitutes
- Shoham Y, Krieger Y, Rubin G, Koenigs I, Hartmann B, Sander F, et al. Rapid enzymatic burn debridement: A review of the paediatric clinical trial experience. Int. Wound J. 2020; 17: p. 1337-1345. Disponible en: https://doi.org/10.1111/iwj.13405
- Korzeniowski T, Struzyna J, Chrapusta A M, Krajewski A, Kucharzewski M, Piorun K, et al. A questionnaire-based study to obtain a consensus from 5 polish burns centers on eschar removal by bromelain-based enzymatic debridement (Nexobrid®) in burns following the 2020 Updated European Consensus Guidelines. J. Pharmacol. Exp. Ther. 2022; 28: e935632. Disponible en: https://doi.org/10.12659/MSM.935632
- Bay C, Chizmar Z, Reece EM, Yu JZ, Winocour J, Vorstenbosch J, Winocour S. Comparison of Skin Substitutes for Acute and Chronic Wound Management. Semin Plast Surg. 2021; 35(3): p. 171-180. Disponible en: doi: 10.1055/s-0041-1731463