ARTÍCULOS

Variabilidad inmunohistoquímica en cáncer de mama: reporte de un caso clínico
Immunohistochemical variability in breast cancer: a clinical case report
Autor:
- Karla Judith Palma Perez (ORCID: 0009-0004-5251-2216)
- Pablo Leonardo Ramos Reyes (ORCID: 0009-0000-8384-1953)
Sobre el autor:
- Doctora en Medicina y Cirugía, UNAH. Residente Tercer año de Oncología
Clínica, Hospital Clínico Quirúrgico Hermanos Ameijeiras, Universidad de Ciencias Médicas de La Habana - Doctor en Medicina y Cirugía, UNAH. Residente Tercer año de Oncología Clínica, Hospital Clínico Quirúrgico Hermanos Ameijeiras, Universidad de Ciencias Médicas de La Habana
Información del manuscrito: Recibido/Received: 28-07-24
Aceptado/Accepted: 20-07-25
Contacto de correspondencia: Leonardoramos04@yahoo.com
Resumen
Los carcinomas de mama representan un grupo heterogéneo de tumores, tanto en su comportamiento clínico como pronóstico. La clasificación se basa en parámetros inmunohistoquímicos (IHQ). Los carcinomas de mama más frecuentes son los de tipo luminal A, carcinomas de tipo luminal B, carcinomas de tipo HER2, carcinomas de tipo basal y los de fenotipo normal. Los carcinomas de mama de tipo luminal mostraron ser, con mayor frecuencia, de forma significativa, tumores bien diferenciados, de pequeño tamaño tumoral, con ganglios axilares negativos, estadio precoz en el momento del diagnóstico, niveles altos de BCL-2 y bajo índice de proliferación con Ki-67. En cambio, los carcinomas de mama de tipo basal y HER2 presentaban tumores de mayor tamaño, pobremente diferenciados, mayor compromiso ganglionar y estadios más avanzados en el momento del diagnóstico. Expresaban con mayor frecuencia índices de proliferación altos con Ki-67 y fueron los subtipos que en curvas de supervivencia global y de supervivencia libre de progresión mostraron una peor evolución. El presente reporte de caso busca analizar las características clinicopatológicas e inmunohistoquímicas y los patrones de supervivencia y recaída de los subtipos presentados. Dentro del cuidado de la salud de la mujer, el cáncer de mama representa nuestro eje de investigación, en proporción de 99:1 respecto al hombre, debido a factores de riesgo. Teniendo en cuenta la dificultad para acceder a los medios diagnósticos (ultrasonografía, mamografía, biopsia) y tratamiento adecuado y oportuno en el sector público del país, lo cual aumenta la morbimortalidad de la mujer.
Palabras clave: neoplasias de la mama, inmunohistoquímica, perfiles moleculares, subtipos de tumor, marcadores tumorales
Abstract
Breast carcinomas represent a heterogeneous group of tumors, both in their clinical behavior and prognosis. Classification is based on immunohistochemical (IHC) parameters. The most common breast carcinomas are luminal A, luminal B, HER2, basal-like, and normal phenotype. Luminal breast carcinomas were shown to be significantly more frequently well-differentiated tumors, with small tumor size, negative axillary nodes, early stage at diagnosis, and high levels of BCL-2 and a low proliferation index with Ki-67. In contrast, basal-like and HER2-positive breast carcinomas presented larger, poorly differentiated tumors with greater lymph node involvement and more advanced stages at diagnosis. They more frequently expressed high proliferation indexes with Ki-67 and were the subtypes that showed the worst outcomes in overall survival and progression-free survival curves. This case report seeks to analyze the clinicopathological and immunohistochemical characteristics and the survival and relapse patterns of the presented subtypes. In women’s healthcare, breast cancer represents our focus of research, with a 99:1 ratio compared to men due to risk factors. Considering the difficulty in accessing diagnostic tools (ultrasonography, mammography, biopsy) and adequate and timely treatment in the country’s public sector, this increases women’s morbidity and mortality.
Keywords: Breast neoplasms, immunohistochemistry, molecular profiling, tumor subtypes, tumor markers
Introducción
El cáncer de mama en el mundo (2022) presentó incidencia global de 2.3 millones de nuevos casos anuales (11.7 % de todos los cánceres). La mortalidad fue de 670 000 muertes/año (6.9 % de mortalidad por cáncer). Las regiones más afectadas fueron América del Norte, Europa Occidental y Australia/Nueva Zelanda (tasas >80/100 000 mujeres). En América Latina y el Caribe la incidencia fue de 210 000 casos nuevos/año (27.7/100 000 mujeres). Con una mortalidad de 57 000 muertes/año (13.5/100 000 mujeres). Cuba tiene mayor incidencia y mortalidad que Centroamérica, similar a países de Sudamérica (ej: Argentina). Honduras muestra tasas más bajas, pero con subregistro y diagnósticos tardíos (60-70 % en etapas avanzadas) (1-5).
El carcinoma de mama representa un grupo de tumores que muestra un comportamiento biológico muy diverso y una gran variabilidad clínica. La clasificación histológica actual de los carcinomas de mama no refleja la heterogeneidad de los tumores en su comportamiento biológico ni permite identificar los pacientes que presentarán mejores respuestas y beneficios con las diferentes modalidades terapéuticas. Actualmente se asume que, la diversidad clínica y pronóstica de carcinomas de mama que son semejantes y homogéneos en cuanto a sus factores pronósticos clásicos, se establece a nivel molecular, al expresar distintos genes que les confieren variabilidad biológica y pronóstica (6).
Durante los últimos años, el estudio de estos genes ha hecho posible, por un lado, comprender el comportamiento biológico del cáncer de mama y, por otro lado, individualizar el pronóstico y el tratamiento de algunos pacientes (6,7). El avance de las tecnologías de análisis genómico ha permitido clasificar los carcinomas de mama en cinco subtipos: luminal A y B, HER2-positivo, basal y similar a la mama normal (6-8).
Los carcinomas de mama de tipo luminal son los subtipos con mejor pronóstico y se caracterizan por expresar el gen del receptor estrogénico, genes asociados (LIV1 y ciclina D1) y queratinas de bajo peso molecular (CK7, CK8, CK18, etc.), de forma semejante al epitelio luminal de los conductos mamarios. Al expresar receptores de estrógenos (RE), estos tumores pueden tratarse con tamoxifeno o inhibidores de la aromatasa, pero muestran una baja respuesta a la quimioterapia neoadyuvante. El carcinoma de mama HER2-positivo muestra expresión aumentada de genes asociados a c-erbB-2 y suele asociarse a otros marcadores de mal pronóstico, incluyendo alteraciones de otros genes como toposio merasa II alfa, GATA4, genes de angiogénesis y proteólisis. Aunque muestran una mejor respuesta a la quimioterapia y cerca de 50 % responde al tratamiento con trastuzumab, el pronóstico es malo (9).
El subtipo basal se caracteriza por la sobreexpresión de citoqueratinas características de la capa basal (CK5/6, CK17) y la expresión de genes relacionados con la proliferación celular. Estos tumores suelen presentar mutaciones en el gen oncosupresor p53, sobreexpresan el receptor del factor de crecimiento epidérmico (EGFR) y se caracterizan por la ausencia de expresión de RE y de genes relacionados y de HER2. Este subtipo se asocia a la mutación BRCA1 y presenta el comportamiento más agresivo a pesar de su alta sensibilidad a la quimioterapia (10).
El carcinoma de mama de tipo normal comparte características del tejido mamario normal, muestra una fuerte expresión de genes normalmente expresados en el tejido adiposo y baja expresión de genes epiteliales luminales. Aunque en el momento actual se considera que el análisis de los perfiles de expresión génica constituye la mejor forma de clasificar los carcinomas de mama, en la mayoría de los hospitales su uso se encuentra limitado ya que son técnicas caras y difíciles de aplicar en material parafinado (11).
En la práctica, la mayor parte de los diagnósticos de rutina se realiza mediante HE y técnicas de inmunohistoquímica (IHQ). Diversos estudios sugieren que, con un limitado número de marcadores inmunohistoquímicos (RE, RP, c-erbB-2, queratinas basales o de alto peso
molecular, queratinas luminales o de bajo peso molecular, P63 y EGFR como marcadores más relevantes) (46), se pueden catalogar los carcinomas de mama en subtipos equivalentes a aquellos basados en perfiles de expresión génica (9-11). La ventaja del estudio IHQ es que utiliza marcadores que se encuentran disponibles en la mayoría de los servicios de Anatomía Patológica y puede aplicarse sobre material archivado del que se puede obtener información clínica y evolutiva.
El objetivo principal de este trabajo es clasificar los carcinomas de mama en subtipos moleculares mediante marcadores inmunohistoquímicos y analizar las características clínicopatológicas e IHQ y los patrones de supervivencia y recaída de los distintos subtipos. Ya que el cáncer de mama es la primera causa de morbimortalidad en mujeres y aumenta la población de escasos recursos y poco acceso a servicios de salud (9-11).
La quimioterapia neoadyuvante es parte integral del tratamiento del cáncer de mama (CM). Hoy su utilización es cada vez más frecuente en estadios iniciales especialmente en los subgrupos HER2+ y triple negativo. Permite aumentar la tasa de cirugías conservadoras, valora la respuesta in vivo al tratamiento y optimiza los tratamientos adyuvantes cuando no se alcanza respuesta patológica completa (PCR) y mejora la supervivencia libre de enfermedad (SLE) en aquellas que la alcanzan (12, 13). Las mayores tasas de PCR se obtienen en los subtipos receptores hormonales negativos/HER2+ (RH-/HER2+) y triple negativo, correlacionándose con un mejor pronóstico en términos de supervivencia libre de enfermedad y global. Por el contrario, la relación entre la tasa de PCR y la SLE es menor en los tumores luminales. En aquellos casos con enfermedad residual, diversos estudios reportan resultados discordantes entre los biomarcadores pre y post neoadyuvancia, en un 15 % para receptores de estrógeno (RE), 30 % receptor de progesterona (RP) y 10 % en los casos HER2+ (12,13).
Existen distintas explicaciones a esta variación como son la heterogeneidad tumoral, cuestiones técnicas, eliminación de clones dominantes debido al tratamiento, y la plasticidad del tumor residual por efecto de la terapéutica instaurada. La poca evidencia en la literatura sobre cómo impacta el cambio del inmunofenotipo en los tratamientos adyuvantes, genera incertidumbre en el manejo de estas pacientes. Sin embargo, distintos grupos recomiendan repetir la determinación de los biomarcadores con el fin de optimizar la indicación de los tratamientos adyuvantes a realizar, maximizando sus beneficios y reduciendo su toxicidad (12-20).
Presentación de caso:
Paciente femenina G.A.R de 37 años, raza blanca, con antecedentes personales patológicos negativos y antecedentes patológicos familiares (madre con cáncer de mama).
Debutó en 2018 con historia de cinco meses de presentar lesión nodular en mama izquierda, en cuadrante superior izquierdo (CSI) se palpa masa redonda de más o menos 3 cm, de contornos duros y no doloroso y no adenopatías. Al examen físico axila negativa.
Se realizó un ultrasonido (USG) que reportó BI-RADS 5. En febrero de 2018, a la décima semana posterior se valoró en consulta de mama y se realizó una biopsia por Trucut (B18-7808), el resultado fue carcinoma infiltrante con IHQ: RE (+) 30 % RPH 30% HER2 (3+). Luminal B y se estadificó como un T2 N0 M0 etapa IIa. Se inició tratamiento con quimioterapia 4AC + 4TX, 3 dosis de paclitaxel y transtuzumab.
Un año después del diagnóstico fue operada de tumorectomía, cuadrantectomía y vaciamiento axilar (VA).
La biopsia postquirúrgica (B19-915) del tejido mamario mostró fibrosis y patrón disperso. Fórmula ganglionar 0/13, sin metástasis. IHQ: RE 30 %, RP 30 %, HER 2 (3+).
Doce semanas luego de la cirugía se decidió tratamiento con tamoxifeno (20 mg), letrozol y transtuzumab (anti HER2) por un año, además recibió radioterapia (RTP) en 15 sesiones. A las ocho semanas de iniciar el tratamiento hormonal (HTP), RTP y anti HER2; mantuvo respuesta completa al tratamiento por más de tres años.
Tres años y dos meses después se realizó un ultrasonido que reportó BIRADS 6, constatando recaída de la enfermedad por un nódulo con BAAF que presentó células atípicas.
Se realizó una cirugía por recidiva, se palpó tumor de aproximadamente 3 cm en CIE que retrae la piel, un mes después, mama derecha y axila sin alteraciones. USG BI-RADS 6 y mamografía BI-RADS 5. Se realizó cuadrantectomía y vaciamiento axilar en mama izquierda.
USG de control mostró nódulo de 1 cm de mama izquierda, lesión dura, bordes irregulares, no dolorosa de 8.3 x 4.3 mm y se realizó biopsia por Trucut (B22-4306): carcinoma ductolobulillar infiltrante, grado nuclear 3. Resultado de marcadores de IHQ: RE negativo, RP negativo, HER2 negativo 0, Ki67 positivo en más del 20 % (40 %), PDL-1 no evaluable.
Se retiró doble bloqueo anti HER2 y se añadió carboplatino 350/m2 + docetaxel (3 ciclos).
Tres meses después de la primera recaída se realizó cirugía mastectomía radical simple de mama izquierda. La herida presentó complicación postquirúrgica de dehiscencia al retirar los puntos 24 horas después. No tuvo respuesta al tratamiento anterior.
Biopsia postquirúrgica (B22-6628): carcinoma ductal infiltrante, moderadamente diferenciado, índice mitótico moderado, grado nuclear II, invasión perineural y premiación tumoral de vasos linfáticos, con fibrosis extensa y áreas con patrón micropapilar, lesión de 1x 0.7x 0.4 cm ubicado en cuadrante inferior externo. Bordes quirúrgicos libres de tumor. No se recibe grasa axilar. RE positivo moderado (70 %), RP positivo intenso (>80 %), HER2 negativo 0, Ki-67 positivo >20 % (40 %). Se propuso continuar con tratamiento hormonal con tamoxifeno (20 mg) por 5 años + goserelina (3.6 mg).
Transcurridos dos meses de la primera recaída, se realizó un USG de mama derecha que reportó un nódulo subcutáneo sobre la herida quirúrgica de 1 cm, BIRADS 4a. No se observa nódulo en la cicatriz quirúrgica de mama izquierda. Por lo cual se considera segunda recaída.
Se realizó biopsia de parche de piel B23-212 que reportó metástasis de piel de alto grado IHQ: RE 10 %, RP 0 %, HER2 0 % Ki67 60 %.
El 9/1/23 cirugía, nódulo Mama derecha + recidiva tumoral en cicatriz de MRM izquierda. Nódulo 1 cm en CSE. Cicatriz de MRM izquierda con 2 nódulos de 0.5 cm en el extremo interno (uno en flap superior y otro en el inferior).
Un mes después de la segunda recaída se realizó recidiva local en mama izquierda postoperado y nódulos en CSE de mama derecha con CAAF con atipia.
Un mes después de la cirugía de la segunda recaída, se realizó exéresis amplia de recidivalocal + exéresis del nódulo subcutáneo + cuadrantectomía radical de mama IHQ luminal B, ganglios positivos (1).
Biopsia B23-1355: metástasis cutánea en cuadrante derecho interno de mama izquierda. Mama derecha: MRM con CDI, grado nuclear 3, metastásico de MI. Mastectomía radical modificada derecha de 22 cm X 16 cm X 4 cm con carcinoma ductal invasor del cuadrante superior externo, talla tumoral de 1 cm X 1 cm X 0.6 cm, grado nuclear 3, grado histológico 3, no es posible descartar la posibilidad de origen metastásico de esta lesión, metástasis en ganglios regionales (1/9), bordes de sección quirúrgica negativos. IHQ: RE positivo débil en el 5 %, RP negativo, HER2 negativo 0, KI67 positivo > 20 % (50 %). B23-212 R: piel de herida: metástasis de piel de carcinoma de alto grado. IHQ RE: positivo débil focal en 10 %, RP negativo, HER2 negativo 0, Ki67 positivo > 20 % (60 %), considerado como tercera recaída. Por lo cual se realizó ooforectomía bilateral, para control hormonal.
A los once meses, recaída local y se inicia tratamiento con capecitabina vía oral durante 6 ciclos en 5 meses. Por no disponibilidad de tratamiento se inició reinducción con carboplatino/paclitaxel, se reevaluaron biopsias anteriores y evidenció positividad para receptores de PDL-1, por lo tanto, se agrega tratamiento anti PDL-1, el cual no culminó los ciclos indicados.
Actualmente con enfermedad oncológica estable y en tratamiento con carboplatino/gemcitabina de mantenimiento.
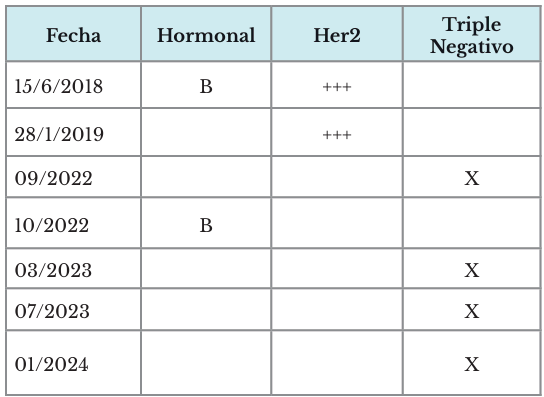
Tabla 1. Fechas y resultados de biopsias
Fuente: Palma Pérez, Ramos Reyes (2025)
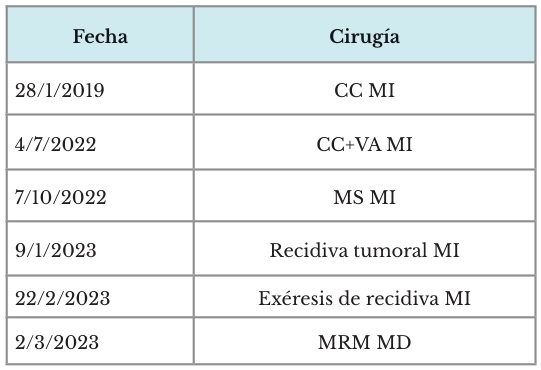
Tabla 2. Cirugías realizadas
Fuente: Palma Pérez, Ramos Reyes (2025)
CC: cuadrantectomía, VA: vaciamiento axilar, MS: mastectomía simple, MRM: mastectomía radical modificada, MI: mama izquierda, MD: mama derecha.
Discusión
El cáncer de mama es un tumor maligno común y la segunda causa de muerte relacionada con el cáncer en las mujeres. La recurrencia y la metástasis del cáncer de mama son las principales causas de muerte.
Es bien reconocida la discordancia del estado de ER, PR y HER2 entre el tumor primario y el tumor recurrente o metastásico; sin embargo, los mecanismos de discordancia siguen siendo desconocidos.
Hay varias explicaciones potenciales para la discordancia en la literatura reportada, incluida la variabilidad en el rendimiento de la detección, la heterogeneidad del tumor y la evolución biológica (17,18). La precisión y confiabilidad de la detección inmunohistoquímica se basan en factores como la fijación del tejido, los métodos de tinción, la selección de antígenos y la interpretación del patólogo. Diferentes períodos, inspectores y métodos podrían afectar los resultados finales (19,20).
Estudios anteriores han demostrado que hay una pequeña cantidad de células cancerosas que son propensas a la recurrencia o metástasis en el cáncer de mama primario. Es posible que estas células no sean detectables en el diagnóstico inicial de cáncer de mama primario y pueden tener características genéticas diferentes (17-21).
Por lo tanto, las pautas de la Red Nacional Integral del Cáncer (NCCN) indican claramente que se necesita una biopsia de lesiones recurrentes y metastásicas para identificar el estado de ER, PR y HER2 de las lesiones recurrentes o metastásicas (22).
Los cambios frecuentes en el estado de ER o PR pueden deberse a la selección o amplificación de diferentes clones de células tumorales debido a mecanismos genéticos o epigenéticos. Durante la terapia endocrina, los niveles de PR disminuyeron significativamente. La literatura consultada demostró que el PR es más variable que la ER en la expresión del cáncer de mama primario y recurrente o metastásico.
En este caso clínico se encontraron cambios similares. Por ejemplo, la tasa de positividad de ER disminuyó y la tasa de positividad de PR disminuyó.
La eliminación de la expresión de PR podría desempeñar un papel importante en el pronóstico, ya que los tumores ER positivos/PR negativos son más invasivos que los tumores ER positivos y PR positivos.
En el curso de la recurrencia o metástasis del cáncer de mama, la expresión del receptor hormonal estuvo parcialmente ausente y la tasa de eliminación de PR en la recurrencia o metástasis fue mayor que la de ER, lo que puede estar relacionado con la heterogeneidad de los tumores y la terapia endocrina previa. Por lo tanto, la ausencia de receptores hormonales en las células tumorales después de la recurrencia o metástasis podría provocar el fracaso del tratamiento en la terapia endocrina de seguimiento (22-24).
El HER2 es uno de los genes importantes relacionados con el cáncer de mama. En muchos estudios se ha demostrado una alta concordancia de HER2 entre tumores primarios y tumores recurrentes o metastásicos. En los casos discordantes, se observó con mayor frecuencia metástasis positivas para HER2 con tumores primarios negativos que lo contrario. En este caso clínico, HER2 cambió de positivo a negativo. La literatura anterior ha demostrado que HER2 se expresa diferencialmente en el cáncer de mama primario y recurrente o metastásico, y si el paciente fue tratado con trastuzumab en el primer diagnóstico es un factor relacionado (25,26).
En aquellos pacientes en los que HER2 cambió de negativo a positivo, se necesitó terapia anti-HER2 adicional. Sin embargo, aún es necesario confirmar si la terapia anti-HER2 es necesaria en pacientes cuyo HER2 cambia de positivo a negativo. Si la recurrencia y la metástasis son clones HER2 negativos, la eficacia de la terapia anti-HER2 sigue siendo controvertida (27).
El índice Ki-67 puede reflejar con precisión la actividad proliferativa de las células tumorales y está relacionado con el desarrollo, la metástasis y el pronóstico de muchos tipos de tumores. En los últimos años se ha ido prestando paulatinamente mayor atención a esta cuestión (23).
El cáncer de mama se puede clasificar en cuatro subtipos moleculares según las características de expresión del receptor y existen diferencias obvias en la consistencia de cada subtipo. Se identificaron tasas de discordancia de expresión más altas con luminal A y B, mientras que se encontró una tasa de discordancia de expresión más baja entre HER2 y Triple negativo (TN) (28).
Además de la escisión quirúrgica y la radioterapia como tratamiento de rescate, esta paciente fue tratada con quimioterapia y terapia hormonal.
Este caso clínico pone en evidencia la necesidad de realizar un seguimiento inmunohistoquímico sistemático en pacientes con cáncer de mama recurrente o metastásico. La variabilidad en la expresión de biomarcadores puede condicionar cambios sustanciales en el abordaje terapéutico. Por tanto, repetir la determinación de RE, RP, HER2 y Ki-67 en cada recaída no solo es clínicamente justificado, sino esencial para una medicina personalizada y efectiva.
Recomendaciones
- Fortalecer el acceso y la repetición sistemática de pruebas inmunohistoquímicas en recurrencias para personalizar tratamientos.
- Desarrollar políticas específicas para poblaciones vulnerables en Honduras que enfrentan barreras de acceso.
- Crear registros nacionales para seguimiento y estudio de patrones moleculares y clínicos.
- Mantener programas de prevención primaria y tamizaje, sin desvincular prevención de diagnóstico temprano y tratamiento oportuno.
La prevención del cáncer consiste en las medidas que se toman para reducir la probabilidad de enfermar de cáncer. Con la prevención del cáncer, se reduce el número de casos nuevos en un grupo o población. Se espera que esto reduzca la carga del cáncer y el número de muertes causadas por esta enfermedad. Lo cual podría ser liderado por el sistema de salud nacional, con programas de salud dirigido a las mujeres, en el cual se les brinde las pruebas de tamizaje, diagnóstico y tratamiento oportuno.
El cáncer no es una sola enfermedad, sino un grupo de enfermedades relacionadas. Nuestros genes, el estilo de vida y el ambiente que nos rodea actúan en conjunto para modificar el riesgo de cáncer, ya sea al aumentarlo o disminuirlo. El riesgo de presentar cáncer en cada persona es una combinación de estos factores. En Honduras hay un amplio número de grupos étnicos, como ser pech, tawahkas, lencas, tolupanes, chortís, misquitos, garífunas y creoles con condiciones socioeconómicas desfavorables. Que históricamente no se han visto alcanzados por el sistema de salud nacional.
Los científicos analizan los factores de riesgo y los factores de protección para prevenir el inicio de cánceres nuevos. Cualquier cosa que aumenta el riesgo de tener cáncer se llama factor de riesgo de cáncer; cualquier cosa que disminuye el riesgo de tener cáncer se llama factor de protección de cáncer.
Aunque algunos factores de riesgo de cáncer se pueden evitar, no es posible evitar muchos otros. Por ejemplo, tanto fumar como heredar ciertos genes son factores de riesgo de algunos tipos de cáncer, pero solo se puede evitar fumar. Hacer ejercicio con regularidad y consumir una alimentación saludable son factores de protección para algunos tipos de cáncer. Es posible que, al evitar los factores de riesgo y aumentar los factores de protección disminuya su riesgo; sin embargo, esto no significa que no enfermará de cáncer. Con políticas de gobierno que promuevan acceso a alimentación saludable, centros recreativos y de ejercicio, espacios libres de humo de tabaco, el Estado no solo estaría promoviendo la salud, sino que también estaría protegiendo a su población de enfermedades graves como el cáncer de mama y haciendo impacto social en la familia.
Las tasas de cáncer de mama en mujeres aumentaron de manera gradual durante muchos años hasta la década de 2000. Las muertes por cáncer de mama disminuyeron un 42 % hasta 2021. Sin embargo, las muertes por cáncer de mama en las mujeres negras siguen siendo un 40 % más altas que en las mujeres blancas. Honduras, al ser un país multiétnico podría hacer un enfoque adaptado a las mujeres que por raza/etnia sufren mayor riesgo de mortalidad y la implicación socioeconómica de una familia sin figura materna (16).
Referencias
- International Agency for Research on Cancer (IARC). Global Cancer Observatory (GLOBO CAN 2022) [Internet]. Lyon: IARC; 2022 [cited 2025 Jul 21]. Available from: https://gco.iarc.fr/
- World Health Organization (WHO). Breast cancer [Internet]. Geneva: WHO; 2023 [cited 2025 Jul 21]. Available from: https://www.who.int/news-room/fact-sheets/detail/breast-cancer
- Pan American Health Organization (PAHO). Cancer in the Americas: Country profiles 2023 [Internet]. Washington, D.C.: PAHO; 2023 [cited 2025 Jul 21]. Available from: https://www.paho.org/en/topics/cancer
- Ministerio de Salud Pública de Cuba. Anuario Estadístico de Salud 2022 [Internet]. La Habana: MINSAP; 2023 [citado 2025 julio 21]. Disponible en: http://www.sld.cu/anuario-estadistico-de-salud/
- Secretaría de Salud de Honduras. Registro Nacional de Cáncer 2020 [Internet]. Tegucigalpa: SSALUD; 2021 [citado 2025 julio 21]. Disponible en: http://www.salud.gob.hn/
- Perou CM, Sørlie T, Eisen MB, van de Rijn M, Jeffrey SS, Rees CA et al. Molecular portraits of human breast tumors. Nature 2000; 406: p. 747-752.
- Sørlie T, Tibshirani R, Parker J, Hastie T, Marron JS, Nobel A et al. Repeated observation of breast tumor subtypes in independent gene expression data sets. Proc Natl Acad Sci U S A. 2003; 100: p. 8418-8423.
- Foekens JA, Atkins D, Zhang Y, Sweep FC, Harbeck N, Paradiso A et al. Multicenter validation of a gene expression-based prognostic signature in lymph node-negative primary breast cancer. J Clin Oncol 2006; 24: p. 1665-1671.
- Nielsen TO, Hsu FD, Jensen K, Cheang M, Karaca G, Hu Z et al. Immunohistochemical and clinical characterization of the basal-like subtype of invasive breast carcinoma. Clin Cancer Res 2004; 10: p. 5367-5374.
- Livasy CA, Karaca G, Nanda R, Tretiakova MS, Olopade OI, Moore DT et al. Phenotypic evaluation of the basal-like subtype of invasive breast carcinoma. Mod Pathol 2006; 19: p. 264-271.
- Burness ML, Grushko T, Olopade OI. Epidermal Growth Factor Receptor in triple-negative and basal-like breast cancer: promising clinical target or only a marker? Cáncer 2010; 16: p. 23-32.
- Ayala, Natalia C; Santana, Verónica S; Alsina, Ángel E; Zimerman, Jorge R; Zimmer mann, María C. Análisis de las variaciones de expresión de marcadores moleculares en cáncer de mama y su relación con cambios de comportamiento tumoral. Libro de artículos científicos en salud [Internet] 2017 [consultado 01 abril 2023]; p. 30-39. Disponible en: https://repositorio.unne.edu.ar/handle/123456789/30261
- Dra. M. D. Ocampo, et al. Cambios en el perfil inmunohistoquímico pre y post neoad yuvancia en el cáncer de mama. Experiencia del Hospital Británico de Buenos Aires. Rev. Argent. de Mastologia [Internet] 2021 [consultado 01 abril 2023]; 40(145) p. 81-98. Disponible en: https://pesquisa.bvsalud.org/portal/resource/pt/biblio-1291292
- M.A. Arrechea Irigoyen, F. Vicente Garcia, A. Codoba Iturruagagoitia, B. Ibanez Beroiz, M. Santamaria Martinez, F. Guillen Grima. Subtipos moleculares del cáncer de mama: implicaciones pronósticas y características clínicas e inmunohistoquímicas. An. Sist. Sanit. Navar[Internet] 2011 [consultado 01 abril 2023]; 34(2) 219-233. Disponible en: https://scielo.isciii.es/scielo.php?pid=S1137-66272011000200008&script=sci_abstract
- Mariangela E. R. Cáncer de mama. Revista Médica Sinergia [Internet] 2018 [consultado 01 abril 2023]; 2(1) p. 8-12. Disponible en: https://revistamedicasinergia.com/index.php/rms/article/view/58/100
- Vicente M. M., Felip G. H. Lesiones histológicas de riesgo de carcinoma de mama. Guía de supervivencia para el patólogo general. Rev Esp Patol [Internet] 2020 [consultado 01 abril 2023]; 53(3) p. 158-166. Disponible en: https://pesquisa.bvsalud.org/portal/resource/pt/ibc-194269
- Jéssica G. F., Carlos U. O. La glándula mamaria, embriología, histología, anatomía y una de sus principales patologías, el cáncer de mama. Revista Médica De Costa Rica Y Centroamérica [Internet] 2012 [consultado 01 abril 2023]; LXIX (602) p. 317-320. Disponible en: https://www.medigraphic.com/cgi-bin/new/resumen.cgi?IDARTICULO=35509
- Raisel G. P., Llanuris L. G., Vicente H. M., María del Carmen A. A., Leticia S. H., Yunexy A. B. Carcinoma de mama triple negativo. Estudio anatomo-estadístico. Medicent Electrón [Internet] 2023 [consultado 01 abril 2023]; 27(1). Disponible en: https://medicentro.sld.cu/index.php/medicentro/article/view/3656
- Gabriela C., et al. Impacto del cambio en el perfil inmunohistoquímico post neoad yuvancia en el tratamiento del cáncer de mama. Experiencia del Hospital Británico de Buenos Aires [Internet]. [consultado 01 abril 2023]. Disponible en: https://ecancer.org/es/journal/article/1162-impact-of-immunohistochemical-profile-changes-following-neoadjuvant-therapy-in-the-treatment-of-breast-cancer/pdf/es
- Planelles A. M. Inmunofenotipos de cáncer de mama en pacientes jóvenes (40 años o menores): estudio de la expresión inmunohistoquímica de la vía IGF1R, PTEN/AKT/mTOR [Tesis doctoral en Internet]. Valencia: Universitat de València; 2012 [consultado 1 abril 2023]. Disponible en: https://dialnet.unirioja.es/servlet/tesis?codigo=68055 Prevención del cáncer de seno (mama). (2013, enero 3). Cancer.gov. https://www.cancer.gov/espanol/tipos/seno/paciente/prevencion-seno-pdq
- Aurilio G, Disalvatore D, Pruneri G, et al. Un metaanálisis de la discordancia del receptor de estrógeno, el receptor de progesterona y el receptor 2 del factor de crecimiento epidérmico humano entre el cáncer de mama primario y las metástasis. Eur J Cáncer 2014; 50: 277-89.
- Siegel RL, Miller KD, Jemal A. Estadísticas de cáncer, 2016. CA Cancer J Clin 2016; 66: p. 7-30.
- Sighoko D, Liu J, Hou N, et al. Discordancia en el estado de los receptores hormonales
- Entre los cánceres de mama primarios, metastásicos y segundos primarios: ¿diferencia biológica o clasificación errónea? Oncólogo 2014; 19: p. 592-601.
- Engel KB, Moore HM. Efectos de las variables preanalíticas en la detección de proteínas mediante inmunohistoquímica en tejido fijado en formalina e incluido en parafina. Arch Pathol Lab Med 2011; 135: p. 537-43.
- Yonemori K, Tsuta K, Shimizu C, et al. Perfiles inmunohistoquímicos de metástasis cerebrales de cáncer de mama. J Neuro-Oncol 2008; 90: p. 223-8.
- Cui X, Schiff R, Arpino G, et al. Biología de la pérdida del receptor de progesterona en el cáncer de mama y sus implicaciones para la terapia endocrina. J Clin Oncol 2005; 23: p. 7721-35.
- Nishimura R, Osako T, Okumura Y. Cambios en los marcadores biológicos ER, PgR, HER2, p53 y Ki-67 entre el cáncer de mama primario y recurrente: tasas de discordancia y pronóstico. Mundial J Surg Oncol 2011; 9: p. 131-8.
- Sun L, Yu DH, Sun SY, et al. Expresiones de ER, PR, HER-2, COX-2 y VEGF en cánceres de mama primarios y en recaída/metastásico. Cell Biochem Biophys 2014; 68: p. 511-6.
- Aitken SJ, Thomas JS, Langdon SP, et al. Análisis cuantitativo de cambios en la expresión de ER, PR y HER2 en cáncer de mama primario y metástasis ganglionares pareadas. Ann Oncol 2010; 21: p. 1254-61.
- Strien L, Leidenius M, von Smitten K, et al. Concordancia entre la expresión del receptor de hormonas esteroides y HER-2 entre el cáncer de mama primario, las metástasis del ganglio centinela y las células tumorales aisladas. Pathol Res Pract 2010; 206: p. 253-8.
- Liu J, Deng H, Jia W, et al. Comparación de los estados de ER/PR y HER2 en sitios metastásicos hepáticos primarios y pareados de carcinoma de mama en pacientes con o sin tratamiento. J Cancer Res Clin Oncol 2012; 138: p. 837-42.
- Yeung C, Hilton J, Clemons M, et al. Discordancia de estrógeno, progesterona y receptor HER2/neu entre tumores de mama primarios y metastásicos: una revisión. Metástasis del cáncer Rev 2016; 35: p. 427-37.